









Категория: Инструкции
Общая характеристика семейства Еnterobacteriaceae
Семейство Enterobacteriaceae является одним из самых обширных и включает наибольшее число патогенных для человека представителей. Местом обитания всех видов энтеробактерий является кишечник, откуда они выделяются во внешнюю среду. Энтеробактерии представляют собой грамотрицательные палочки средних размеров. Спор не образуют. По типу дыхания относятся к факультативным анаэробам. Подвижны благодаря перитрихиально расположенным жгутикам или неподвижны при их отсутствии. Хорошо растут на простых питательных средах. Все представители семейства Enterobacteriaceae обладают сахаролитической активностью – ферментируют углеводы до кислоты и газа или только до кислоты. Протеолитическая активность выражена слабо. В биохимическом отношении наиболее активна Escherichia coli, являющаяся представителем нормальной микрофлоры организма человека. Наименьшей ферментативной активностью обладают Shigella dysenteriae и Salmonella typhi.
Дифференцирующие признаки энтеробактерий на среде Клиглера:Среда Клиглера содержит:
МПА ( Мясо-пептонный агар -мясопептонный бульон +агар-агар)
Принцип действия среды: ферментация глюкозы происходит только в анаэробных условиях в глубине среды (столбика) из-за ее малой концентрации. Ферментация лактозы происходит в аэробных условиях на поверхности среды (скоса). При этом цвет индикатора меняется на желтый (закисление среды). О продукции сероводорода узнаем по почернению среды.
1.Эшерихии.Таксономия и классификация
Царство: Procaryota;Отдел: Gracilicutes;Семейство: Enterobacteriaceae;Род: Esherichia;Вид: Esherichiacoli.
Морфология и тинкториальные свойства
Эшерихии палочки средних размеров. Грамотрицательны, большинство подвижны благодаря перитрихиально расположенным жгутикам, но есть и неподвижные варианты. Спор не образуют. Некоторые штаммы имеют капсулу.
Факультативные анаэробы. Растут при температуре от 10° до 46°С, оптимальная температура 35 - 37°С. Хорошо растут на простых питательных средах образуя колонии средних размеров, гладкие, влажные, блестящие, с ровным краем. На жидких средах вызывают равномерное помутнение, иногда с осадком или пленкой. В окружающей среде эшерихии устойчивы. При 60°С погибают в течение 15 мин. В воде, почве сохраняют жизнеспособность в течение нескольких месяцев. Прямой солнечный свет вызывает гибель через несколько минут. Чувствительны к действию дезинфицирующих веществ.
Эшерихии высоко активны – ферментируют углеводы, в т.ч. лактозу, до кислоты и газа. Протеолитическая активность выражена слабо, могут продуцировать индол. Большинство эшерихий лактозоположительны поэтому на среде Эндо (МПА + лактоза + фуксин) образуют темно-красные колонии с металлическим блеском, не ферментирующие лактозу эшерихии, растут в виде бесцветных колоний.
Сложная: соматический О-антиген, капсульный К-антиген и жгутиковый Н-антиген. О-антиген (171 разновидность) определяет серологическую группу. Поверхностный К-антиген представлен 3 вариантами – А, В и L. Они отличаются друг от друга по термоустойчивости. Самым термостабильным является А-антиген – он выдерживает кипячение в течение двух часов. В-антиген выдерживает воздействие температуры 60°С в течение часа. L-антиген разрушается при нагревании до 60°С. К-антиген располагается более поверхностно, чем О-антиген, поэтому он может препятствовать агглютинации О-сыворотками. В этом случае О-антиген можно выявить только после разрушения К-антигена кипячением в течение двух часов. Типовой специфичностью обладает Н-антиген, по которому эшерихии делятся на серологические варианты (около 60).
По патогенности вид E.coli не является однородным. Различают:
непатогенные (резидентные) комменсалы. пожизненно колонизирующие толстый кишечник;
условно -патогенные – вызывают внекишечные поражения (цистит, сепсис); такие заболевания возникают, как правило, эндогенно за счет эшерихий, колонизирующих кишечник;
патогенные (диареегенные) эшерихии – вызывают острые кишечные инфекции (ОКИ), которые имеют экзогенное происхождение.
Условно-патогенные эшерихии входят в состав нормальной микрофлоры кишечника. Являются санитарно-показательными микроорганизмами (присутствие кишечной палочки в воде, почве, пищевых продуктах, предметах обихода свидетельствует о их фекальном загрязнении). Условно-патогенные эшерихии способны вызывать заболевания при проникновении в ткани вне пищеварительного тракта - в мочевыводящие и желчные пути, легкие, брюшину, мозговые оболочки, где возникает гнойно-воспалительный процесс, который нередко развивается на фоне иммунодефицита.
ПатогенныеE. сoli– возбудители ОКИ, получили названиедиареегенных. Они подразделяются на 4 основные категории:
энтеротоксигенные E. сoli (ETEC);
Энтеротоксигенные эшерихии (ETEC). Серогруппы: О6, О8, О15, О20, О25, О27, О63, О78, О80, О85, О115, О128ас, О139, О148, О153, О159, О167 являются возбудителями холероподобного заболевания у детей и взрослых, известного под названием «диарея путешественников». Кодируемые плазмидой термолабильный (LT) и термостабильный (ST) энтеротоксины нарушают водно-солевой обмен в кишечнике, приводя к развитию водянистой диареи. Клиническая картина инфекции сходна с холерой: водянистая диарея, тошнота, рвота, кишечные спазмы, небольшая лихорадка. В испражнениях примеси отсутствуют или обнаруживается небольшое количество слизи. Вспышки водные, пищевые. Сезонность летняя. Название «диарея путешественников» отражает факт частого возникновения данных инфекций у вновь прибывших в неблагополучный регион лиц, тогда как местное население постоянно контактируя с возбудителями (инфицированная вода, продукты) имеет иммунитет.
Энтероинвазивные эшерихии (EIEC). Серогруппы: О28ас, О29, О124, О136, О143, О144, О152, О164, О167. Способны внедряться и размножаться в клетках эпителия нижнего отдела подвздошной и толстой кишки. Являются возбудителями дизентериеподобных заболеваний, характеризующихся непродолжительной водянистой диареей, развитием колитического синдрома, лихорадкой, токсикозом. В стуле возможна примесь крови, слизи, полиморфноядерных лейкоцитов. Обычно болеют дети в возрасте от 1,5 до 2 лет, но могут болеть и подростки, и взрослые. Сезонность летне-осенняя. Вспышки пищевые, водные. Заболевания нередко регистрируются как госпитальная инфекция, при этом доминируетE. сoli О124.
Энтеропатогенные эшерихии (EPEC). Эта группа эшерихий включает 9 серогрупп класса 1: О55, О86, О111, О119, О125, О126, О127, О128аb, О142 и четыре серогруппы класса 2: О18, О44, О112, О114. Вирулентность этой группы эшерихий связана с белком наружной мембраны, получившим название интимин, его синтез детерминирован хромосомным геном, а также белком, синтез которого контролируется плазмидой 60 мДа. Некоторые серовары продуцируют шигаподобные токсины. ЕРЕС обладают способностью размножаться на поверхности эпителия тонкого кишечника, что приводит к разрушению микроворсинок и повреждению апикальной поверхности эпителия. Заболевание характеризуется продолжительной водянистой диареей, рвотой, лихорадкой, симптомами обезвоживания. Часто имеет место тяжелое, пролонгированное течение. В стуле обнаруживается примесь слизи. Инфекция передается преимущественно контактно-бытовым путем. Преимущественно болеют дети в возрасте до двух лет. Сезонность не выражена. Вспышки бытовые, редко пищевые. Часто регистрируются как внутрибольничные инфекции в отделениях для новорожденных и грудных детей, находящихся на искусственном вскармливании.
Энтерогеморрагические эшерихии (EHEC). Серогруппы: О26, О111, О145, О157. Наибольшее эпидемиологическое значение имеетE. сoli серовара О157:Н.
ЕНЕС способны к адгезии на поверхности клеток эпителия толстой кишки. Адгезия обусловлена пилями, детерминированными плазмидой размером 60 мДа. Эта плазмида, кроме этого, детерминирует синтез гемолизина, способствующего нарушению барьерной функции кишечника. Развитие геморрагического колита обусловлено способностью эшерихий данной группы продуцировать шигаподобные токсины (их синтез контролируется конвертирующими фагами). Поражаются слепая, восходящая и поперечная толстая кишка. Клинически заболевание проявляется колитическим синдромом, отсутствием лихорадки. В испражнениях наблюдается обилие крови, но без полиморфноядерных лейкоцитов. Около 5% больных погибает, у 12 – 30% возникают тяжелые осложнения, включая почечную недостаточность, гипертонию, поражение центральной нервной системы. Сезонность летне-осенняя. Поражаются все возрастные группы за исключением грудных детей.
Экология и распространение
Естественным местом обитания эшерихий является кишечник человека, животных, большинства птиц, многих пресмыкающихся, рыб, насекомых. Открыты в 1885 г. австрийским педиатром Т. Эшерихом искавшим возбудителя «детской холеры».
Эпидемиология, патогенез и клиника заболевания (особенности )
Гастроэнтерит новорожденных - тяжелое, часто смертельное заболевание.Диарея взрослых - от легких форм, сопровождающихся жидким стулом, недомоганием, до тяжелой холероподобной формы болезни. Эти заболевания встречаются повсеместно, однако чаще среди некачественно питающихся групп населения. Источник инфекции человек, больной или носитель. Механизм передачи фекально-оральный, пути передачи- пищевой, водный, бытовой.Аутоинфекции.Инфекция мочевого тракта. Е. coli - самый распространенный возбудитель воспаления мочевого пузыря (цистит), реже почек (пиелонефрит). Инфекция преимущественно восходящая - из уретры в мочевой пузырь и почечные лоханки. Штаммы, вызывающие эти заболевания, отличаются по некоторым свойствам, например, по способности образовывать фимбрии, которые служат у них фактором адгезии.Бактериемия — тип генерализованного процесса, вызываемого E.coli. Иногда этот тип инфекции встречается при внутрибольничном заражении. Бактериемия может исходить из абсцессов в брюшной полости, мозге, костях.
Основной метод диагностики – бактериологический. Исследуемым материалом может служить гнойное отделяемое раны, моча, кровь, при острых кишечных инфекциях – фекалии. Материал засевают на среду Эндо. По морфологическим, культуральным и биохимическим свойствам патогенные и непатогенные эшерихии не отличаются друг от друга, поэтому отбор подозрительных колоний проводят по антигенной структуре:на стекле ставят реакцию агглютинации с поливалентными адсорбированными коли-сыворотками и материалом из колоний. Если на чашке вырастают колонии одного типа (на среде Эндо – малиново-красные, с металлическим блеском), агглютинируют не менее 10 колоний. Если обнаруживаются колонии разных типов (малиново-красные без металлического блеска, темно-розовые и т.п.), то испытывают с помощью реакции агглютинации по 5 колоний каждого типа. Чистую культуру выделяют из колоний, давших положительную реакцию агглютинации с поливалентной коли-сывороткой. Идентификацию выделенных культур проводят путем изучения ферментативной активности и антигенной структуры. Определяют серологическую группу с живой и гретой культурой и О- и К-сыворотками. Для выявления О-антигена культуру эшерихий кипятят на водяной бане в течение 1 – 2 часов, что приводит к разрушению К-антигена.
Методические указания
по санитарно-бактериологическому контролю на предприятиях общественного питания и торговли пищевыми продуктами
(утв. заместителем Главного государственного санитарного врача СССР 31 декабря 1982 г. № 2657)
Санитарно-бактериологический контроль является ценным вспомогательным методом при санитарном обследовании объектов, дающим возможность объективно оценивать уровень санитарного содержания обследуемых предприятий общественного питания и торговли.
Применение унифицированных методов исследования позволяет получать сравнимые достоверные данные, характеризующие санитарное благополучие отдельного участка предприятия в целом или ряда предприятий, а также обобщать эти данные.
По результатам санитарно-бактериологических исследований можно судить о соблюдении санитарного режима на предприятии, о возможном нарушении технологии приготовления пищи или условий хранения продуктов, о соблюдении правил личной гигиены персоналом, об эпидемиологической безопасности готовой продукции и др.
Таким образом, санитарно-бактериологический контроль незаменим при проведении санитарных обследований предприятий общественного питания и торговли и поэтому является обязательным для использования в практике повседневной работы санитарно-эпидемиологических станций и ведомственных санитарно-пищевых лабораторий.
- конечная цель - профилактика пищевых отравлений бактериальной природы и острых кишечных инфекций путем обеспечения выпуска в предприятиях общественного питания и реализации в продовольственных магазинах доброкачественных и безопасных в эпидемическом отношении пищевых продуктов;
- ближайшая цель - выявить причины выпуска на производстве или при реализации в торговой сети продуктов, недоброкачественных или опасных в эпидемическом отношении, и способствовать ликвидации этих причин.
- критерием высокого качества санитарной обработки оборудования, посуды, инвентаря и др. служит отсутствие на поверхности обработанных предметов санитарно-показательных, а также патогенных микроорганизмов;
- обнаружение значительной микробной обсемененности готовых продуктов сапрофитной микрофлорой должно расцениваться как показатель санитарного неблагополучия объекта;
- выявление высокой обсемененности готовых продуктов санитарно-показательными микроорганизмами следует расценивать, как указание на возможность заражения этих продуктов патогенными микроорганизмами;
- обнаружение патогенных микроорганизмов в готовых выпускаемых или реализуемых продуктах (в определенных количествах продукта) расценивается как показатель эпидемического неблагополучия объекта;
- результаты санитарно-бактериологических исследований следует сравнивать с показателями стандартов или рекомендаций по допустимому уровню обсемененности продуктов микроорганизмами.
Санитарно-бактериологические исследования проводятся:
а) при плановых санитарных обследованиях объектов общественного питания и торговли, осуществляемых в порядке текущего санитарного надзора;
б) при обследованиях объектов в порядке предупредительного санитарного надзора с целью гигиенической оценки технологической линии производства новых видов пищевых продуктов (блюд); новых типов технологического и торгового оборудования, а также при вводе в эксплуатацию новых или реконструированных предприятий;
в) при санитарных обследованиях объектов в арбитражном порядке;
г) по санитарно-эпидемиологическим показаниям *(1) ;
*(1) При возникновении пищевых отравлений исследования проводятся в соответствии с действующей «Инструкцией о порядке расследования, учета и проведения лабораторных исследований в учреждениях санитарно-эпидемиологической службы при пищевых отравлениях», № 1135-73.
д) внеплановые - при санитарных обследованиях предприятий по заданиям вышестоящих организаций и др.
а) готовые блюда, кулинарные изделия, скоропортящиеся и особо скоропортящиеся пищевые продукты в предприятиях общественного питания и торговли;
б) в отдельных случаях сырье и полуфабрикаты (по ходу технологического процесса - по эпидпоказаниям, при высокой бактериальной обсемененности готовых продуктов, блюд и др.);
в) оборудование, инвентарь, посуда и др. с целью проверки эффективности санитарной обработки;
г) смывы с рук, санитарной одежды, личных полотенец (с целью проверки соблюдения правил личной гигиены персоналом);
д) вода центрального водоснабжения и особенно - местных источников водоснабжения (места водозабора и краны).
Первоочередному контролю подлежат объекты питания, на которых приготовление пищевых продуктов или отдельные этапы технологического процесса являются наиболее опасными в санитарно-эпидемиологическом отношении, а также предприятия, неблагополучные по санитарно-техническому состоянию. Например, требуют большего внимания объекты, вырабатывающие кулинарные, кондитерские кремовые изделия или другие особо скоропортящиеся пищевые продукты (паштеты, селедочное масло, заливные, студни и др.), также более тщательного наблюдения требуют объекты, находящиеся в неудовлетворительном санитарно-техническом состоянии, затрудняющем нормальную эксплуатацию и поддержание должного санитарного режима на предприятии (неполный набор помещений, недостаточная их площадь, недостаток холодильников, перебои с горячей и холодной водой, плохая работа канализации и т.д.).
В торговой сети первоочередному обследованию, главным образом, подлежат специализированные магазины или секции продовольственных магазинов, реализующие особо скоропортящиеся товары (молоко и молочные продукты, мясные и рыбные кулинарные изделия, кремовые изделия и др.).
Санитарное обследование с отбором проб для лабораторных исследований проводится санитарным врачом или его помощником в присутствии руководителя предприятия или замещающего его лица без предварительного оповещения.
Результаты исследований отражают качество пищевых продуктов, позволяют выявить нарушения санитарного содержания предприятий, обнаружить уязвимые точки, потенциально опасные в отношении загрязнения продукции, дать ответ на вопрос о причинах и источниках загрязнения продукции, характеризовать уровень санитарной культуры персонала, намечать пути устранения выявленных недостатков.
Каждое обследование оформляется актом в 2-х экземплярах по установленной форме, который подписывается лицом, производящим обследование и руководителем предприятия.
Результаты каждого обследования должны быть доведены до сведения администрации и персонала предприятия и обсуждены на производственном совещании предприятия не позднее 3-х дней после завершения исследований. Обобщенные результаты лабораторных исследований следует периодически обсуждать на совещаниях в вышестоящих организациях (трестах, столовых, торгах, УРСах) или других организациях, которым подчиняются предприятия.
На основании данных санитарно-бактериологического обследования предприятий администрацией должны быть разработаны конкретные меры по устранению выявленных недостатков с обязательной последующей проверкой санэпидстанциями эффективности проведенных мероприятий.
План проведения санитарно-бактериологического контроля предприятий общественного питания и торговли должен составляться санитарными врачами оперативных отделений СЭС совместно с лабораторными работниками. При планировании устанавливается количество объектов, подлежащих санитарно-бактериологическому контролю, кратность их обследования - с учетом возможностей лаборатории *(2). Санитарно-бактериологические обследования должны проводиться в соответствии с утвержденными графиком при этом для обследуемых объектов должен сохраняться принцип внезапности. Рекомендуемая кратность планового обследования предприятий:
*(2) - Кратность обследования может изменяться в зависимости от общего числа пищевых объектов, подконтрольных данной СЭС, значимости объектов, эпидобстановки и др. но не реже, чем указано в «Нормативах проведения основных санитарно-бактериологических исследований объектов окружающей среды» (методические указания), М. 1983, Утв. МЗ СССР № 2671-83.
а) в теплое время года (при температуре наружного воздуха +10 °С и более) -
- благополучные объекты - 1 раз в месяц для предприятий общественного питания и 1 раз в 2 месяца для предприятий торговли;
- эпидзначимые (неблагополучные) - 2 раза в месяц для предприятий общественного питания и 1 раз в месяц для предприятий торговли;
б) в холодное время года (при температуре наружного воздуха ниже +10 °С)
- благополучные объекты - 1 раз в 2 месяца для предприятий общественного питания и 1 раз в 4 месяца для предприятий торговли;
- эпидзначимые объекты - 1 раз в месяц для предприятий общественного питания и 1 раз в 2 месяца для предприятий торговли.
Отбор проб и смывов должен производиться санитарным врачом или помощником санитарного врача. В необходимых случаях отбор проб и смывов целесообразно производить совместно с работниками лаборатории, чтобы обеспечить правильность их проведения.
При отборе проб пищевых продуктов, методики исследования которых предусмотрены соответствующими ГОСТ, ОСТ, ТУ и СТ СЭВ, следует руководствоваться указаниями раздела «отбор проб», а в случае отсутствия - специальным стандартом по правилам отбора проб и настоящими Методическими указаниями, а кроме того, учитывать конкретные обстоятельства на обследуемом объекте.
Перед выемкой проб продуктов представитель санэпидстанции должен ознакомиться с имеющейся на данную партию продукта документацией (накладные, сертификаты и т.п.); произвести наружный осмотр всей партии, обращая внимание на состояние тары (исправность, деформации, загрязнение и т.п.); внешний вид продукта; условия хранения (реализации) и транспортировки. При обнаружении неисправности тары, могущей повлиять на качество продукта, следует производить вскрытие каждой неисправной единицы упаковки (за исключением случаев, оговоренных в стандартах).
После осмотра партии производится вскрытие отдельных единиц упаковки и выемка проб для органолептического исследования на месте и для исследования в лаборатории.
Количество единиц упаковки, подлежащих вскрытию, устанавливается действующими стандартами, ОСТ, ТУ и т.п. на соответствующие продукты.
При осмотре продуктов, на которые стандарты или ТУ отсутствуют, вскрывают до 5 % единиц упаковки от общего их количества в партии, но не менее 5 единиц.
В процессе отбора проб составляется акт отбора проб по установленной форме (№ 342-у - для пищевых продуктов, № 344-у - для кулинарных изделий), в котором указывается: дата и час взятия проб, точное наименование обследуемого предприятия, место и точка отбора (участок, цех, рабочее место и т.п.), подробное описание взятой пробы и т.п.
Составляется точное направление на исследование по форме № 378-у.
2.7.1. Отбор проб готовых блюд на предприятиях общественного питания и продуктов, реализуемых в торговой сети.
Исследованию подлежат следующие готовые блюда и продукты:
а) холодные блюда:
- винегреты и салаты из вареных овощей и фруктов;
- мясные и рыбные студни, заливные;
- печеночные и мясные паштеты;
- масло селедочное, сырое и с др. наполнителями;
- холодные мясо и рыба;
- мясная и рыбная кулинария;
б) первые холодные блюда:
- ботвинья, свекольник и др.;
в) вторые горячие блюда:
- изделия из мясного или рыбного фаршей (котлеты, биточки, шницели, тефтели и др.);
- изделия из мелко нарезанного мяса (гуляш, рагу, азу и др.);
изделия из субпродуктов;
г) гарниры (к вторым горячим блюдам):
- макаронные изделия отварные;
- овощные и др. гарниры;
- компоты из сухих и свежих фруктов, кисели;
- сбитые сливки, муссы, желе и т.п.;
- напитки, изготовленные в предприятиях общественного питания;
е) кондитерские изделия с кремом;
з) продовольственные товары:
- молоко и молочные продукты (кефир, сливки, сгущенное молоко, мороженое, сметана, творог, творожная масса);
- сыры сычужные и плавленые;
- колбасные изделия, особенно вареные, ливерные и субпродуктовые, свинокопчености;
- рыбные продукты (икра), рыбная гастрономия;
- яичный порошок, яичный меланж;
- напитки минеральные, безалкогольные, слабоалкогольные, пиво;
- вина бочковые и в оригинальной упаковке;
- жиры: масло сливочное, топленое, маргарин;
- кондитерские изделия (карамель, пастила, мармелад, печенье);
Исследования горячих блюд проводятся для определения остаточной микрофлоры с целью проверки эффективности термической обработки, а также вторичного обсеменения в процессе реализации. Исследования холодных блюд проводят для определения общего количества микроорганизмов, титра бактерий группы кишечных палочек - с целью установления вторичного обсеменения в процессе приготовления или реализации этих блюд.
Оценка качества особо скоропортящихся пищевых продуктов и блюд по результатам бактериологических анализов производится в соответствии с «Временными рекомендациями по микробиологическим нормативам для ряда особо скоропортящихся пищевых продуктов и методам их исследования», утвержденными Минздравом СССР 30/ХII 1981 г. за № 2510-81.
2.7.2.1. Отбор проб пищевых продуктов при обследовании технологического процесса производства.
Если по результатам бактериологических исследований установлено, что отдельные блюда, пищевые продукты оказываются систематически обсемененными санитарно-показательными микроорганизмами, то проводят санитарно-бактериологическое обследование производства данного блюда или продукта по ходу технологического процесса, чтобы установить этап, на котором происходит обсеменение продукта микрофлорой. Целесообразно параллельно с отбором проб продуктов на разных этапах технологического процесса делать смывы с оборудования, инвентаря и посуды, с которыми соприкасался продукт.
Например, при обследовании процесса приготовления салата или винегрета бактериологическому исследованию подвергаются все исходные компоненты, входящие в состав блюда, по этапам их обработки: вареные овощи - после их охлаждения и очистки, далее - после измельчения; вареное мясо - после охлаждения, после измельчения; исследуется также зеленый горошек и др. компоненты блюда. Затем берут пробу блюда после перемешивания всех компонентов, но без заправки и квашеных овощей. Заправку исследуют отдельно. Одновременно производятся смывы с инвентаря и оборудования, разделочных досок, ножей, крышки стола, овощерезок, посуды, рук работников холодного цеха.
2.7.2.2. Техника отбора проб.
Для отбора проб продуктов и блюд в лаборатории заготавливаются отдельные банки, закрытые двумя слоями бумаги и обвязанные бечевкой, стерильные ложки, стерильные пинцеты и ножи, завернутые в бумагу.
Пробы продуктов рекомендуется отбирать вдвоем с привлечением в качестве помощника представителя обследуемого учреждения. Помощник в одной руке держит банку, другой - по мере необходимости открывает крышку. В это время лицо, отбирающее пробу, развертывает требующуюся ложку или пинцет, берет материал и переносит в банку. При необходимости отбора пробы от большого куска, отрезают часть его с помощью стерильного ножа и пинцета.
Если проба блюда берется в раздаточной, то в банку переносят с тарелки всю порцию; если образец отбирают на производстве от большой массы продукта (из кастрюли, от большого куска мяса), то берут пробу весом около 200 г, жидкие блюда - после тщательного перемешивания; плотные - из разных мест в глубине куска. Напитки минеральные, безалкогольные, слабоалкогольные и пиво отбирают в количестве 1 бутылки заводской упаковки и 200 мл напитка, изготовленного на предприятии.
2.7.3. Санитарно-бактериологический контроль методом исследования смывов
В практике текущего санитарного надзора за объектами общественного питания, торговой сети, пищеблоками детских, дошкольных и подростковых учреждений, а также буфетами-раздаточными лечебно-профилактических учреждений (в том числе санаториев, домов отдыха и др.) широко используется метод смывов с целью контроля эффективности санитарной обработки инвентаря, оборудования, посуды, санитарной одежды и рук персонала. Метод смывов дает возможность объективно оценить санитарное содержание обследуемых учреждений.
При проведении санитарно-бактериологических исследований смывов в основном ограничиваются выявлением бактерий группы кишечных палочек, обнаружение их расценивают, как одно из подтверждений нарушения санитарного режима.
При выявлении вторичного массивного обсеменения готового продукта со значительным превышением в нем общего количества микробов, в смывах также необходимо определять общую бактериальную обсемененность и наличие бактерий рода Proteus и St. aureus.
Особое внимание при проведении смывов уделяют контролю оборудования и аппаратуры, которые используются по ходу технологического процесса приготовления продуктов, не подвергающихся в дальнейшем тепловой обработке (холодный цех).
Бактериологический контроль методом смывов с поверхностей инвентаря, оборудования, рук и санитарной одежды персонала может преследовать две цели:
а) установить эффективность санитарной обработки, для этого смывы с инвентаря, оборудования, рук и санитарной одежды персонала производят перед началом работы, или, если это невозможно, в перерывах, после того, как руки и оборудование подверглись санитарной обработке, т.е. смывы производят с чистых объектов. Кроме того, смывы с рук берутся у персонала после посещения туалета до возобновления работы;
б) определить роль оборудования и рук персонала в бактериальном обсеменении продукта или готового блюда по ходу технологического процесса производства, обращая особое внимание на производство продуктов и готовых блюд, прошедших термическую обработку или употребляемых в пищу без предварительной обработки (некоторые овощи, гастрономические продукты, салаты, винегреты и др.). Для решения поставленной задачи одновременно со взятием смывов отбирают повторные пробы пищевых продуктов (смывы берутся с необработанных рук и поверхностей).
Количество подконтрольных объектов, кратность их обследования, количество доставляемых смывов определяются не только мощностью лаборатории, конкретными условиями каждой санэпидстанции, но и эпидситуацией, которая может иметь решающее значение.
В случае необходимости более подробного санитарно-бактериологического обследования отдельных участков производства, например, проверки качества мытья столовой посуды и приборов, режима приготовления блюд, взятие проб и смывов производится по специальной программе, составленной для каждого конкретного объекта. Непосредственно на предприятии при каждом обследовании устанавливают конкретные точки для взятия смывов. При повторных обследованиях следует брать смывы с тех же объектов и по возможности в те же часы.
При взятии смывов с оборудования, инвентаря, посуды, столовых приборов записывается: номер образца по порядку, место взятия смыва, в каком техническом и санитарном состоянии находилось оборудование (инвентарь, посуда и т.п.), с которого взят смыв.
При взятии смывов с рук записывается: номер по порядку, фамилия, имя и отчество сотрудника, выполняемая работа (профессия и участок работы).
Составляется акт о взятии смывов в 2-х экземплярах, подписывается лицом, отобравшим пробы и представителем администрации предприятия. 1 экземпляр акта оставляется на объекте. Результаты исследования доводятся до сведения руководителя предприятия в течение 5 дней.
Доставка проб должна производиться в термоконтейнерах (с охлаждаемыми вкладышами).
Время доставки проб продуктов и смывов в лаборатории для осуществления исследования не должно превышать 2-х часов, так как затягивание этого срока отражается на достоверности результатов анализа.
При взятии смывов необходимо пользоваться следующими рекомендациями:
1) Из оборудования следует обращать внимание на разделочные доски, мясорубки, производственные столы для готовой пищи, особенно в цехе приготовления холодных закусок. Смывы в цехах производства кондитерских кремовых изделий производят в соответствии с «Методическими указаниями по проведению санитарно-бактериологических исследований на предприятиях, вырабатывающих кондитерские кремовые изделия», М. 1976.
2) Смывы с рук, с санитарной одежды, полотенец берутся в основном у работников, имеющих дело с продукцией, не подвергающейся в дальнейшем тепловой обработке (персонал кухни, холодного цеха, раздатчицы, буфетчицы, официанты, продавцы). Порядок определен разделом 2.7.3.. п. «а».
3) Смывы с крупного оборудования и инвентаря берут с поверхности в 100 см 2. для ограничения поверхностей используют шаблон (трафарет), сделанный из проволоки, металлической пластинки. Трафарет имеет площадь 25 см 2. чтобы взять смывы с площади в 100 см 2. его накладывают 4 раза в разных местах поверхности контролируемого объекта.
4) При взятии смывов с мелких инструментов обтирается вся поверхность предмета, при заборе смывов с тарелок протирают всю внутреннюю поверхность. При взятии смывов с мелких предметов одним тампоном протирают три одноименных объекта - три тарелки, три ложки и т.п. У столовых приборов протирают их рабочую часть.
5) При исследовании стаканов протирают внутреннюю поверхность и верхний наружный край стакана на 2 см вниз.
6) При взятии смывов с рук протирают тампоном ладонные поверхности обеих рук, проводя не менее 5 раз по каждой ладони и пальцам, затем протирают межпальцевые пространства, ногти и подногтевые пространства.
7) При взятии смывов с санитарной одежды протирают 4 площадки по 25 см 2 - нижнюю часть каждого рукава и 2 площадки с верхней и средней частей передних пол спецовки. С различных мест полотенца берут 4 площадки по 25 см 2 .
Взятие смывов производится с помощью стерильных увлажненных ватных тампонов. Стерильные ватные тампоны на стеклянных, металлических или деревянных палочках, вмонтированых в пробирки с ватными пробками, заготавливают заранее в лаборатории. В день взятия смывов в каждую пробирку с тампоном наливается (в условиях бокса над горелкой) по 5 мл стерильного 0,1 % водного раствора пептона или изотонического раствора хлорида натрия таким образом, чтобы ватный тампон не касался жидкости.
Непосредственно перед взятием смыва тампон увлажняют наклонением пробирки или опусканием тампона в жидкость. В процессе отбора смывов рекомендуется неоднократное смачивание тампонов.
При плановом санитарно-бактериологическом контроле пищевых продуктов подлежат исследованию:
- количество мезофильных аэробных и факультативно анаэробных микроорганизмов (МАФАнМ) - (общее количество микробов) *(3) ;
*(3) - Общее количество микробов не определяют в продуктах, содержащих специфическую микрофлору: кисломолочных продуктах, заправленных салатах, винегретах в квашеными овощами, поскольку подсчет бактерий в таких случаях не может быть показательным.
- количество бактерий группы кишечных палочек (БГКП) *(4). а в части продуктов - количество БГКП методом наиболее вероятного числа (НВЧ);
*(4) - В тех случаях, когда коли-титр меньше 1, целесообразно характеризовать обсемененность исследуемого жидкого продукта в виде коли-индекса.
- коагулазоположительные стафилококки (St. aureus);
- бактерии рода Proteus;
- бактерии рода Salmonella в 25 г продукта.
Количество мезофильных аэробных и факультативно-анаэробных микроорганизмов (МАФАнМ), количество бактерий группы кишечных палочек, St. aureus и Proteus определяют нижеизложенными методами. Исследование на отсутствие или наличие сальмонелл проводится в соответствии с действующей «Инструкцией о порядке расследования, учета и проведения лабораторных исследований в учреждениях санитарно-эпидемиологической службы при пищевых отравлениях», № 1135-73 .
Содержание или отсутствие в определенной массе исследуемого продукта вышеперечисленных микроорганизмов должно соответствовать нормативам, изложенным во «Временных указаниях по микробиологическим нормативам для ряда особо скоропортящихся пищевых продуктов и методам их исследования», № 2510-81. При наличии ГОСТа на методы бактериологического анализа (например, ГОСТ 9958-81 «Изделия колбасные и продукты из мяса») анализ проводят в соответствии с ГОСТ, а для оценки качества продуктов пользуются «Временными указаниями» № 2510-81.
В тех случаях, когда по ГОСТу используется для анализа навеска продукта, превышающая норматив, (например, в ГОСТ 9958-81 бактерии группы кишечных палочек в зельцах определяют в 1 г, а во «Временных указаниях» № 2510-81 норматив для зельца белого I с и серого II с - отсутствие БГКП в 0,5 г), то делается заключение о соответствии качества продукции по микробиологическим показателям, если БГКП не обнаруживаются в 1 г продукта.
Если БГКП обнаруживают в 1 г, то бактериолог СЭС имеет право сделать посев навески массой 0,5 г.
При разработке ГОСТов на негостированную продукцию общественного питания и пересмотре действующей нормативно-технической документации необходимо руководствоваться методами, изложенными в настоящих «Методических указаниях».
4.1. Подготовка проб пищевых продуктов к бактериологическому исследованиюПищевые продукты подразделяются по физическим свойствам на плотные и жидкие, следовательно, и способы обработки их перед исследованием должны быть различными. Перед исследованием пробы вначале подготавливают навеску, которая должна охарактеризовать всю доставленную пробу. Навески продукта берут в условиях бокса стерильно из разных мест пробы, с поверхности и из глубины.
Подготовка навески проб пищевых продуктов, на которые имеется ГОСТ на методы исследования, осуществляется в соответствии с требованиями последних.
Для продуктов, не имеющих ГОСТ на методы исследования, (вторые блюда, гарниры, каши, винегреты), отбирают навеску в количестве 15 г на технических весах I класса из усредненной пробы.
Навеску плотных продуктов растирают в стерильной фарфоровой ступке с песком или гомогенизируют в микроразмельчителе тканей с постепенным добавлением 135 мл 0,1 % раствора пептона в воде или изотонического раствора хлорида натрия и оставляют при комнатной температуре на 15 минут. Затем для посевов взвесь отбирают стерильной пипеткой с широким концом. Принимается, что 1 мл приготовленной взвеси содержит 0,1 г исходного продукта.
Продукты жидкой консистенции - молоко, компоты, напитки, изготовленные в объектах общественного питания, засевают без предварительной обработки; пищевые продукты, имеющие кислую реакцию (рН 4,0 - 6,0), перед исследованием нейтрализуют стерильным 10 % раствором двууглекислого натрия до слабощелочной реакции (рН 7,2 - 7,4). Реакцию среды проверяют с помощью рН-метра или по универсальной индикаторной бумаге.
Для исследования на сальмонеллы из усредненной пробы отбирается отдельная навеска массой 25 г.
4.2. Приготовление разведений пищевых продуктов для посеваДля пищевых продуктов жидкой и полужидкой консистенции, не требующих предварительного размельчения и растирания, разведения готовят следующим образом:
Берут ряд пробирок (обычно не более 5-ти), каждая пробирка должна содержать 9,0 мл стерильного 0,1 % раствора пептона или изотонического раствора натрия хлорида. В первую пробирку стерильной градуированной пипеткой вносят 1,0 мл исследуемого продукта, затем новой стерильной пипеткой после весьма тщательного перемешивания содержимое 1-й пробирки в количестве 1 мл переносят в следующую пробирку, не прикасаясь к поверхности жидкости в этой пробирке и т.д.
В результате исследуемый продукт оказывается разведенным в 10, 100, 1000 и более раз в соответствии с количеством взятых пробирок. 1 мл взвеси в первой пробирке содержит 0,1 г (мл) продукта (1-е разведение), во второй пробирке - 0,01 г (мл) продукта (2-е разведение) и так далее.
При исследовании пищевых продуктов плотной консистенции в качестве первого разведения используют 10 %-ю взвесь, полученную после механической обработки продукта в ступке или гомогенизаторе, описанным выше способом (п. 4.1. ).
4.3. Метод определения количества мезофильных аэробных и факультативно анаэробных микроорганизмов в 1 г (мл) продукта - (Общее микробное число ОМЧ) - «МАФАнМ»Метод основан на способности мезофильных аэробов и факультативных анаэробов расти на питательных средах определенного состава при температуре 30 °С с образованием колоний, видимых при увеличении в 2 раза.
Для определения количества мезофильных бактерий следует выбирать разведения, при посеве которых на чашках вырастает на менее 30 и не более 300 колоний.
Из каждой пробы делают посев глубинным методом на 2 параллельные чашки Петри из 2 - 3 последовательных разведений в количестве 1,0 мл, используя для этого 2 %-й агар, приготовленный из сухого питательного агара (см. стр. 44). Контролировать температуру надежнее и проще, если агар разливают небольшими порциями в пробирки (12 - 15 мл). Агар в пробирках быстрее расплавляется и охлаждается более равномерно до нужной температуры. Чашки заливают расплавленным и остуженным до 45 °С агаром сразу же после внесения материала. В противном случае может наблюдаться неравномерное распределение колоний в виде отдельных скоплений в толще агара; для более равномерного распределения посевного материала, кроме того, содержимое чашки перемешивают вращательными движениями.
После застывания агара чашки с посевами помещают в термостат дном вверх, инкубируют по рекомендации ФАО/ВОЗ при 30 °С в течении 72 часов; при необходимости предварительный учет производят через 48 часов. Количество колоний подсчитывается на каждой из засеянных чашек. Счет колоний на чашках производят с помощью прибора для счета колоний бактерий или лупы. Для лучшей видимости считают колонии на темном фоне (под чашку кладут темную бумагу), чашки помещают дном кверху. Каждую колонию отмечают на дне чашки чернилами или тушью.
При подсчете придерживаются следующих правил:
а) если на чашке выросло небольшое количество колоний, примерно 100, подсчитывают все колонии;
б) если колонии распределены равномерно и их количество измеряется несколькими сотнями (200 - 300 колоний), допускается подсчет колоний не менее чем на 1/3 площади чашки. В этих случаях дно чашки делят карандашом на 6 секторов и считают колонии в 3 секторах. Затем делают пересчет на всю площадь чашки: вычисляют среднее количество колоний на площади одного сектора и полученное количество колоний на одном секторе умножают на 6;
в) если на чашке вырастает более 300 колоний, они распределены равномерно и не представляется возможным повторить анализ, то, применяя прибор для счета колоний бактерий, подсчитывают 10 полей зрения площадью по 1 см 2 в разных местах чашки. Полученные числа складывают и выводят среднее арифметическое. Чтобы высчитать количество колоний на всей чашке, полученное среднее число умножают на площадь чашки (Пи R2). Обычно диаметр чашки равен 8,5 - 10 см, Пи = 3,14. Подставив данные в формулу, получаем при диаметре чашки, равном 10 см, площадь чашки 78,5 см 2. При отсутствии прибора для счета колоний бактерий можно использовать обычную миллиметровую бумагу, в которой вырезают «окошко» площадью 1 см 2. Подсчет колоний производят с лупой, как указано выше.
Пример, если среднее число колоний на 1 см 2 составляет 18, диаметр чашки 10 см, то число колоний на всей площади чашки 18 × 78,5 = 1413, округляя в ответе, указывают 1400.
Число колоний, выросших на чашке, должно отражать количество жизнеспособных микроорганизмов, содержащихся в засеянном объеме исследуемого материала. Поскольку последний, как правило, засевают в разведенном виде, число выросших на чашке колоний умножают на степень взятого разведения, рассчитывают среднее арифметическое и устанавливают количество мезофильных аэробных и факультативно анаэробных микроорганизмов в 1 г (мл) продукта.
При установлении количества мезофильных бактерий не все чашки могут быть использованы для вычисления среднего арифметического:
а) нельзя использовать посевы для вычисления среднего арифметического, если количество выросших колоний на чашках менее 30. В этом случае в протокол исследований вносят показатели обсемененности, полученные при подсчете колоний только по одной или двумя чашкам, число колоний на которых больше 30. В случае роста колоний на засеянных чашках в количестве менее 30, в результатах анализа рекомендуется следующая формулировка: «Рост единичных колоний при посеве (указать количество засеянного продукта)».
б) не используются посевы для вычисления среднего арифметического показателя на тех чашках, на поверхности которых более чем на 1/2 площади отмечается ползучий рост спорообразующих микроорганизмов, последние могут маскировать рост прочих бактерий. Возможны случаи, когда на чашках из всех разведений получен рост споровых микроорганизмов, и подсчет изолированных колоний практически не возможен. В этих случаях в протоколе исследования следует указывать: «Рост спорообразующих микроорганизмов».
Пример расчета: Если на чашках Петри при посеве 0,1 г продукта выросло в среднем 135 колоний, а при посеве 2-го разведения (0,01 г продукта) - 9 колоний, то в результатах исследования учитывают цифровые данные, полученные при посеве 1-го разведения, т.е. количество микроорганизмов 135 × 10 = 1350 в 1 г продукта.
Для получения более точных данных по количеству мезофильных бактерий, целесообразно сопоставлять результаты подсчета колоний, полученные на чашках в посевами материала из последовательных разведений. Числа подсчитанных колоний должны примерно соответствовать кратности взятых разведений. Если количество колоний на чашках с посевами из последующих разведений (1:10, 1:100) почти совпадает или мало между собой разнится, то это указывает на недостаточное перемешивание посевного материала при приготовлении разведений и перед посевом.
Для приведения в соответствие показателя «бактерии группы кишечных палочек» с принятой международной номенклатурой (Coliformes - ФАО/ВОВ и СЭВ), а также с действующими ГОСТ 2874-82 («Вода питьевая») в настоящих «Методических указаниях» к бактериям группы кишечных палочек отнесены грамотрицательные, не образующие спор палочки, сбраживающие лактозу с образованием кислоты и газа при температуре 36 °С ± 1 °С.
При необходимости производится дальнейшее исследование с идентификацией до E. coli.
В тех случаях, когда на продукт имеется норматив - отсутствие бактерий группы кишечных палочек в определенной массе продукта (альтернативный показатель), то результат записывается в соответствии с количеством продукта, подвергнутого микробиологическому анализу. Например, «бактерии группы кишечных палочек в 1 г - отсутствуют».
В тех случаях, когда продукт должен содержать сравнительно низкие количества БГКП - не выше 10(3) - (например, диетические молочные продукты - творог, сметана детская диетическая и т.д.), определение БГКП проводят методом наиболее вероятного числа (НВЧ).
В тех случаях, когда на продукт имеется действующий ГОСТ, предусматривающий норматив по коли-титру, или необходимо выявить значительную степень загрязнения продукта БГКП, определяют их коли-титр.
4.4.1. Методика посева продуктов при альтернативном определении БГКП
Для посева используется то количество продукта, в котором в соответствующей НТД предусматривается отсутствие БГКП. При этом продукты жидкой консистенции (напитки, кисели, компоты) засевают непосредственно в среду Кесслер с лактозой (с поплавком) или в среду КОДА, соблюдая соотношение продукта и среды 1:10. Продукты плотной консистенции подготавливают к посеву в соответствии с п. 4.1. Посевы помещают в термостат при температуре 37 °С на 24 часа. При отсутствии признаков роста - газообразования или изменения цвета среды дают заключение о соответствии исследованного продукта нормативу (например, БГКП в 1 г отсутствуют). При наличии признаков роста на среде КОДА дают заключение о несоответствии продукта нормативу на БГКП. При наличии признаков роста на среде Кесслер с лактозой необходимо для окончательного заключения о присутствии в продукте БГКП произвести высев из газ-положительных пробирок на чашки со средой Эндо. Чашки помещают в термостат с температурой 37 °С на 18 - 20 часов. Посевы просматривают. Из колоний, подозрительных или типичных для БГКП, готовят мазки, окрашивают по Граму и микроскопируют. Обнаружение грамотрицательных палочек указывает на наличие БГКП.
4.4.2. Определение количества бактерий группы кишечных палочек методом наиболее вероятного числа - НВЧ (Coliformes - ФАО/ВОЗ и СЭВ)
Группа колиформных бактерий включает все аэробные и факультативно анаэробные грамотрицательные неспорообразующие палочки, ферментирующие лактозу с образованием кислоты и газа в течение 24 - 48 часов при 36 °С ± 1 С, относящиеся к E. coli, Citrobacter, Enterobacter, Klebsiella и Seratia. В связи с тем, что в п. 4.1.1. настоящих «Методических указаний» принято определять БГКП по ферментации лактозы при 36 °С ± 1 С в течение 24 - 48 часов, то группы микроорганизмов, относящиеся к «колиформным бактериям» и БГКП, в настоящих «Методических указаниях» максимально сближены и по существу являются идентичными.
Поэтому метод определения НВЧ для колиформных бактерий отражает и определение наиболее вероятного числа БГКП в исследуемом объеме продукта.
4.4.2.1. Ход исследования.
Гомогенат, приготовленный по п. 4.1.. или жидкий продукт, разведенный 1:10, набирают в пипетку в количестве 1,0 мл и переносят в пробирку, содержащую 9 мл 0,1 % пептонной воды или изотонического раствора хлорида натрия, смешивают осторожно, набирая и выдувая из пипетки 10 раз, получая т.о. разведение продукта 1:100. Затем готовят разведения 1:1000, перенося каждый раз стерильной пипеткой 1 мл из приготовленного разведения в следующую пробирку с 9 мл 0,1 % пептонной воды. Осторожно встряхивают все разведения.
Вносят по 1 мл разведения продукта 1:10 в 3 пробирки с 10 мл среды КОДА. Таким же образом производят посев двух последующих разведений 1:100 и 1:1000, используя для этих целей каждый раз чистую стерильную пипетку.
Посевы инкубируют при 36 °С ± 1 С в течение 24 часов.
Регистрируют все пробирки, показавшие образование газа или изменение цвета среды через 24 часа. Пробирки без признаков роста инкубируют еще 24 часа и затем регистрируют те пробирки, где есть признаки роста. Затем проводят тест, подтверждающий наличие БГКП в исследуемом продукте, для чего переносят одну полную петлю из каждой положительной пробирки со средой КОДА в отдельные пробирки с желчно-лактозным бульоном, содержащим бриллиантовую зелень (п. 6.6. ) - средой ЖЛБ, и инкубируют эти пробирки при 37 °С в течение 24 - 48 часов. По образованию газа в поплавках регистрируют число положительных пробирок, которые подтверждают наличие БГКП.
4.4.2.2. Расчет наиболее вероятного числа (НВЧ) БГКП.
Наиболее вероятное число БГКП рассчитывается в зависимости от количества пробирок с положительной пробой на газообразование в ЖЛБ по таблице 4.4.2.3. Например, положительное газообразование отмечено в 3-х пробирках посева разведения 1:10, в 1 пробирке посева разведения 1:100 и 0 пробирок из разведения 1:1000. Из таблицы видно, что НВЧ для такой комбинации положительных реакций равно 43 бактериям в 1 г продукта. В заключении указывают: «1 г или 1 мл продукта содержит 43 БГКП».
4.4.2.4. Определение E. coli по методу НВЧ.
При необходимости определения наличия E. coli в исследуемом на БГКП продукте по методу НВЧ одновременно с подтверждающим пересевом на ЖЛБ с бриллиантовой зеленью может быть сделан пересев из всех пробирок с наличием признаков роста на среде КОДА на среду Кесслер с лактозой или на среду для E. coli (п. 6.7 ) - КС-бульон. Засеянные пробирки инкубируют при 44 °С ± 1 °С 24 часа и регистрируют образование газа.
Таблица пересчета НВЧ и пределы с 95 % вероятности при использовании 3-х пробирок
Число положительных пробирок с разведениями
Для дефференциации выделенных культур применяют реакции на индол, метил-рот, Фогэс-Проскауэр и цитрат.
Из пробирок с положительной реакцией (образование газа) штрихом производят посев на чашку с агаром Левина таким образом, чтобы получить изолированные колонии, и инкубируют 18 - 24 часа при 37 °С.
Переносят 2 - 3 колонии с каждого выросшего посева на среде Левина на чашку или пробирку с 2 % МПА и инкубируют 18 - 24 часа при 37 °С. В то же время из каждой культуры готовят мазки и производят окраску по Граму.
Постановка тестов ИМАЦ
Культуру со скошенного агара инокулируют в пробирку с 5 мл индольной среды (п. 6.10. ) и инкубируют при 37 °С в течение 24 часов. Добавляют 1 мл индольного реактива. При наличии индола в пограничном слое в течение 5 мин появляется красное окрашивание - положительная реакция.
Реакция Фогес-Проскауэра (на ацетилметилкарбинол)
Культуре со скошенного агара петлей вносят в пробирку с 5 мл среды Кларка (п. 6.12. ). Посев инкубируют при 37 °С в течение 48 часов. Затем к 1 мл культуры, перенесенному в другую пробирку, добавляют 0,6 мл этанолнафтольного реактива и 0,2 мл раствора КОН. Встряхивают после добавления каждого реактива, читают реакцию через 15 минут. Учет результатов возможен и через 2 часа. Окраска от розовой до ярко-красной показывает, что реакция на образование ацетилметилкарбинола положительная.
Тест на метил-рот.
Инокулируют пробирку со средой Кларка и инкубируют в течение 48 часов при 36 °С ± 1 °С (параллельно с постановкой реакции на ацетилметилкарбинол), в оставшиеся после постановки реакции Фогеса-Проскауэра 4 мл культуры добавляют 4 - 5 капель индикатора метил-рот в каждую пробирку. Реакция ферментации углеводов с образованием кислоты положительная, если появилось красное окрашивание.
Тест с утилизацией цитрата.
Культуру с МПА пересевают в пробирку со средой Козера (цитратной) или на чашку со средой Симмонса, инкубируют 96 часов при 37 °С и проверяют рост. Отсутствие роста и изменения цвета среды - реакция отрицательная. Наличие роста, изменение окраски среды с оливково-зеленого цвета на васильковый свидетельствует об утилизации цитрата - реакция положительная.
Классификация бактерий группы кишечных палочек по тестам ИМАЦ
Используя табл. 4.4.2.5. принимают, что E. coli - это грамотрицательные, неспорообразующие палочки, образующие газ из лактозы и дающие положительную или отрицательную реакцию на индол, положительную - с метил-рот и отрицательные реакции Фогеса-Проскауэра и на цитрат - -(+ - -) или (- + - -). Количество E. coli в 1 г рассчитывают по таблице 4.4.2.3.. учитывая число положительных пробирок со средой Кесслер с лактозой или ЕС-бульоном, инкубированных при 44 °С ± 1 °С. В заключении указывают: «В 1 г (мл) продукта «N» E. coli.»
Схема 1.
Определение количества бактерий группы кишечных палочек методом НВЧ
1. Гомогенат продукта
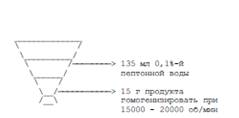
2. Разведение гомогената продукта

3. Предварительный тест. Инкубация при 37 °С 24 - 48 ч.

4. Подтверждающий тест. Инкубация при 37 °С 48 ч.
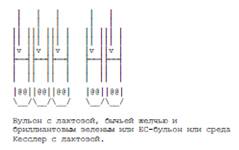
5. Регистрация пробирок с наличием газа и расчет НВЧ по таблице.
4.4.3. Метод определения коли-титра БГКП.
Под коли-титром следует понимать наименьшее количество исследуемой пробы, выраженное в мл (воды, жидкие пищевые продукты) или в г (плотные пищевые продукты), в котором обнаруживается присутствие бактерий группы кишечных палочек.
При определении титра кишечных палочек выявляют их наличие в различных объемах исследуемого продукта.
При наличии стандартных методов подвергают исследованию те количества продукта, которые предусмотрены соответствующими ГОСТ, весь ход исследования, сроки и температура выращивания, а также количественный и качественный учет кишечных палочек должен соответствовать ГОСТ на тот или иной пищевой продукт.
4.4.3.1. Методика посева пищевых продуктов, не имеющих ГОСТ *(5) .
*(5) - В тех случаях, когда на исследуемый продукт имеется микробиологический показатель, то засевается соответствующее количество продукта (п. 4.4.1.).
Первый этап: Первичные посевы на среду накопления.
Засевают 4 или более десятикратно убывающих количеств пищевого продукта, например 10,0; 1,0; 0,1; 0,01 мл (Г).
В качестве среды накопления применяют среду Кесслер с лактозой или среду КОДА. Среды разливают в пробирки не менее чем по 5 мл для посева малых объемов (1 мл, г и менее). Для посева объема от 10 мл и более среду разливают во флаконы по 50 - 100 мл (применение поплавков не обязательно). Для определения титра бактерий группы кишечных палочек засевают в среду Кесслер исходную 10 %-ю взвесь в количестве 100 мл (10 г продукта) во флакон со 100 мл среды двойной концентрации, 10 мл (1 г продукта) - во флакон с 50 мл среды, 1,0 (0,1 г продукта), а также 1,0 мл из разведения 1:100 (0,01 г продукта) и т.д. - в пробирки с 5,0 мл среды. Посевы выдерживают в термостате при 37 °С 16 - 24 часа.
Второй этап. Посев на плотную среду Эндо.
Из всех пробирок с посевами на среде Кесслер или КОДА независимо от помутнения среды, производят посевы на сектора чашек со средой Эндо (при отсутствии среды Эндо пользуются средой Левина). Для получения изолированных колоний берут петлей минимальное количество материала при значительном помутнении среды Кесслер и производят посев частым штрихом. Чашки с посевами помещают в термостат при 37 °С на 16 - 24 часа.
Чашки с посевами на среде Эндо просматривают. При отсутствии характерных колоний на всех секторах чашки дают ответ - «титр бактерий группы кишечных палочек более 11,1». При наличии на среде Эндо колоний, характерных для бактерий группы кишечных палочек - красных с металлическим блеском или без него, розовых с темным центром, розовых, слизистых, бледно-розовых, производят их изучение *(6) .
*(9) - тесты на окисление маннита, термоустойчивую ДНКазу, кислую фосфатазу проводят в случае отрицательной реакции плазмокоагуляции.
Из изолированных колоний, характерных для бактерий группы кишечных палочек, готовят препараты, окрашивают по Граму и микроскопируют. В случае обнаружения в препарате смешанной культуры, выбирают другую колонию и производят рассев на чашку со средой Эндо для получения чистой культуры. При отсутствии в мазках грамотрицательных палочек дают ответ - «титр бактерий группы кишечных палочек выше 11,1».
Заключение о наличии бактерий группы кишечных палочек только по внешнему виду колоний, без их изучения, недопустимо.
В случае обнаружения в препаратах грамотрицательных палочек исследование продолжают. Из проверенных колоний грамотрицательных палочек производят высевы на среду Гисса с глюкозой, разлитую в пробирки с поплавками. При наличии однотипных колоний грамотрицательных палочек на всех 4-х секторах чашки со средой Эндо допускается высев колоний на среду Гисса с глюкозой из двух последних секторов (разведений). Инкубация при 37 °С 18 - 24 часа. Для ускорения анализа высевы из колоний производят в пробирки с небольшим количеством подогретой до 37 °С среды (1,5 - 2,0 мл). Пробирки с посевами ставят в термостат при 37 °С и просматривают через 5 - 6 часов роста. Наличие кислото- и газообразования в них указывает на присутствие бактерий группы кишечных палочек в том или ином засеянном объеме; пробирки с посевами, не забродившими через 4 - 6 часов, вновь помещают в термостат при 37 °С и выдерживают до 16 - 24 ч.
4.4.3.2. Учет результатов.
Для установления коли-титра применяют стандартные таблицы. Пользование таблицами возможно только при определенном количестве засеянных объемов. Чаще всего для пищевых продуктов, на которые не имеется ГОСТ, используются таблицы, рассчитанные на посевы 4 десятикратно убывающих количеств от 10,0 г до 0,01 г. Если предполагается более интенсивное обсеменение продукта бактериями группы кишечных палочек, то производят посевы больших разведений от 0,001 до 0,00001 г и для вычисления титра бактерий группы кишечных палочек пользуются таблицами 4.4.3.4. ; 4.4.3.5. ; 4.4.3.6. в зависимости от того, в каком разведении еще обнаруживается рост кишечных палочек, заканчивая учет двумя последними разведениями, в которых имеется наличие (в предпоследней) и отсутствие (в последней пробирке) роста бактерий группы кишечных палочек. Например, 0,1+; 0,01+; 0,001+; 0,0001-. В данном случае следует пользоваться таблицей 4.4.3.5. Для данной комбинации результатов коли-титр равняется 0,0004.
Таблицы для вычисления коли-титра в продуктах
Объемы: 10,0; 1,0; 0,1 и 0,01 мл
Клетки стафилококков сферические, 0,5 - 1,5 мкм в диаметре. В результате деления более чем в одной плоскости образуют гроздьевидные скопления. Неподвижные, грамположительные. Образуют внеклеточные ферменты и токсины. Температурный оптимум 35 - 40 °С. пределы для роста 6,5 - 46 °С. Оптимум рН 7,0 - 7,5, пределы рН для роста - 4,2 - 9,3. Стафилококки активно образуют пигмент (липохром) золотистый, эмалево-белый, лимонно-желтый, особенно при комнатной температуре (20 °С) и при доступе воздуха. Колонии стафилококков на плотных средах имеют форму правильных дисков от 2 до 4 мм в диаметре. Края колонии ровные, поверхность слегка выпуклая, блестящая, непрозрачная, окрашена в цвет пигмента. В жидких средах дают сильное диффузное помутнение, образуя постепенно осадок. Согласно последней классификации (Берги, 1980) род Staphylococcus включает три вида: Staph. aureus, St. epidermidis, St. saprophyticus. Стафилококки, относящиеся ко всем трем видам, могут быть причиной различных заболеваний человека, а стафилококки, вырабатывающие энтеротоксины, при определенных условиях могут вызывать пищевые интоксикации. В настоящее время Sasph. aureus целесообразно использовать в качестве санитарно-показательного микроорганизма при исследовании пищевых продуктов, а также при обследовании объектов общественного питания, особенно пищеблоков в детских дошкольных и подростковых учреждениях для оценки их санитарного содержания.
4.5.1. Методика количественного определения Staph. aureus.
Методика выделения St. aureus предусматривает его количественное определение в пищевых продуктах и наличие его в смывах.
1 этап: Из исходной 10 % взвеси продукта производят посев на элективные среды: желточно-солевой (ЖСА) или молочно-солевой (МСА) агары. Основную 10 % взвесь в количествах 0,5 и 0,1 мл (0,05 и 0,01 г продукта) наносят на поверхность среды, равномерно распределяют и тщательно растирают шпателем. Кроме этого, 1 мл исходной взвеси (0,1 г продукта) засевают в пробирки с 5 мл 6,5 %-го солевого бульона. Продукты жидкой консистенции высевают на плотные среды в количестве 0,5 и 0,1 мл, а в жидкие - 1,0 мл. Продукты с пониженной водной активностью (аw 0,86) или с повышенным содержанием поваренной соли дополнительно засевают также в количестве 1,0 мл (0,1 г, мл продукта) на сахарный бульон, разлитый в пробирки по 5 мл.
Посевы инкубируют при 37 °С в течение 18 - 24 часов, чашки с плотными средами оставляют еще на сутки при комнатной температуре *(7) .
*(7) - На средах, содержащих желток, стафилококк, выделенный от человека, образует у 60 - 70 % выделенных культур венчик вокруг колонии (положительная лецитовителлазная реакция). Стафилококки животного происхождения дают положительную лецитовителлазную реакцию в 5 - 10 % культур.
2 этап. а) Просматривают посевы на МСА или ЖСА, на ЖСА колонии стафилококков дают радужный венчик, на МСА - образуют пигмент: золотистый, кремовый, эмалево-белый и др. Изолированные колонии, подозрительные на стафилококк, изучают, микроскопируют с окраской по Граму и высевают на скошенный МПА или на сектора чашки с молочным агаром. Число колоний, взятых для идентификации, должно быть не менее 5 - 7.
б) Из сред обогащения производят высевы на сектора чашки с молочным агаром.
Все посевы инкубируют при 37 °С в течение 18 - 24 часов.
3 этап: Выделенную чистую культуру с секторов на чашках с молочным или из пробирок со скошенным МПА подвергают микроскопии с окраской по Граму. При наличии мелких грамположительных кокков ставят реакцию плазмокоагуляции.
4.5.2. Постановка реакции плазмокоагуляции.
Наилучшим методом предварительной идентификации St. aureus в лабораторных условиях является коагулазная проба в пробирке, закрытой ватной пробкой, с кроличьей или человеческой плазмой. При чтении реакции плазмокоагуляции установлено 3 градации активности фермента коагулазы:
1) ++++ - сгусток плотный, 2) +++ - сгусток, имеющий небольшой отсек, 3) ++ - сгусток в виде взвешенного мешочка.
Эту реакцию следует читать очень осторожно, чтобы не повредить и не нарушить начало ее образования.
Постановка реакции: В пробирку с 0,5 мл цитратной плазмы, разведенной изотоническим раствором натрия хлорида в соотношении 1:4, вносят петлю суточной культуры стафилококка и ставят в термостат при 37 °С. Осторожно просматривают реакцию плазмокоагуляции через 30 минут, 1 час, 2 - 4 часа и оставляют до утра при комнатной температуре для окончательного учета. Ускорение реакции производят за счет использования 3 - 4 часовых бульонных культур, добавляя их в количестве 0,1 мл к 0,5 мл разведенной плазмы.
После полного подтверждения принадлежности выделенных штаммов к St. aureus производят подсчет колоний на плотной среде и устанавливают содержание стафилококков в 1 г (мл) исследуемого продукта.
4.5.3. Определение St. aureus в особо скоропортящихся продуктах, имеющих микробиологический норматив *(8) .
*(8) - «Временные указания по микробиологическим нормативам для ряда особо скоропортящихся пищевых продуктов и методам их исследования», М. 1982 г. Утв. МЗ СССР 30/XII-81 г. № 2510-81.
В ряде продуктов общественного питания, микробиологические нормативы предусматривают отсутствие St. aureus в 0,1 г и в 1,0 г продукта.
В тех случаях когда отсутствие St. aureus предусматривается в 0,1 г продукта, необходимо 1 мл 10 %-й взвеси продукта, приготовленной в соответствии с п. 4.2.. внести в 9 мл солевого бульона (6,5 % aCl). В тех случаях, когда отсутствие St. aureus предусматривается в 1 г продукта, для этих целей усредненная проба массой в 10 г растирается в стерильной ступке и отсюда делается навеска на стерильном часовом стекле или стерильном пергаменте массой 1,0 г и засевается в 9 мл солевого бульона.
Посевы инкубируют при 37 °С в течение 18 - 24 часов. После чего из солевых бульонов производят подтверждающий посев петлей на сектора чашки Петри с желточно-солевым агаром или молочно-солевым агаром. Инкубацию посевов производят при 37 °С в течение 18 - 24 часов. После чего чашки просматривают. При отсутствии роста типичных колоний для St. aureus делают заключение об отсутствии этого микроорганизма в исследуемой навеске продукта (в 1,0 г или 0,1 г).
При наличии роста подозрительных на стафилококки колоний производят их изучение, как в п. 4.5.1. (этапы 2 и 3), п. 4.5.2 .
При наличии коагулазоположительных St. aureus делают заключение о присутствии этого микроорганизма в исследуемой навеске продукта. Следовательно, данный продукт не соответствует требуемому нормативу - «отсутствие St. aureus в 1,0 или в 0,1 г продукта».
4.5.4. Дополнительные тесты идентификации.
При наличии санитарно-эпидемического неблагополучия следует использовать дополнительные тесты. Прежде всего еще раз уточнить реакцию плазмокоагуляции, с этой целью культуру пересевают 2 - 3 раза на скошенном МПА и повторяют постановку реакции, или рассевают культуру на чашках с мясо-кептонным агаром для проведения повторной идентификации из новых колоний стафилококков. В случае неудовлетворительных результатов целесообразно из первичных посевов взять ряд других колоний и подвергнуть их вновь идентификации.
Если выделенную культуру не идентифицировали как St. aureus, следует использовать дополнительные тесты: постановку реакции на термостабильную ДНКазу, окисление маннита, фосфатазу, лецитовителлазу.
4.5.4.1. Тест на лецитовителлазу
При использовании для первичного посева среды, содержащей желток, специального, дополнительного определения лецитовителлазной активности у стафилококков проводить на следует. В случае выделения культур с других сред и необходимости определения у них этого признака на чашку с желточным агаром сеют испытуемую культуру штрихом или бляшкой - последнее экономнее. Чашки инкубируют при 37 °С в течение 18 - 20 часов. При положительном результате вокруг колонии стафилококка образуется радужный венчик, что обусловлено выделением фермента лецитовителлазы и разложением лецитина, находящегося в среде. Реакцию следует учитывать в отраженном свете.
4.5.4.2. Реакция на разложение маннита в анаэробных условиях
Используют среду, приготовленную из сухого препарата с индикатором ВР и маннитом, разливают в пробирки по 10 мл, стерилизуют при 0,7 атм 20 минут. Перед посевом среду освобождают от воздуха, для чего пробирки кипятят в водяной бане при 100 °С 10 минут, затем быстро охлаждают в ледяной воде и немедленно производят посев уколом. Сверху засеянную среду заливают расплавленным 2 % водным агаром слоем 2 - 3 см, чтобы исключить попадание воздуха. Посевы термостатируют при 37 °С в течение 4 дней. Просмотр осуществляют на 2 и 4 дни. Результаты расценивают как ферментацию маннита, когда нижняя и верхняя части среды четко изменяют цвет из зеленого на синий. В этом случае микроорганизмы идентифицируют как St. aureus. Если посинеет только верхняя часть среды, то имеет место окисление маннита. Если спустя 4 дня инкубации на произошло посинения, сбраживания маннита на произошло. В 2-х последних случаях микроорганизмы относят к St. epidermidis или St. saprophyticus.
4.5.4.3. Определение активности кислой фосфатазы
Среда: к 100 мл 2 % МПА, расплавленного и остуженного до 45 °С, добавляют 50 мг паранитрофенилфосфата натрия, разливают в чашки Петри. Посев производят бляшками - до 20 бляшек на чашку. Реакцию можно учитывать уже через 2 часа инкубации при 37 °С. Вокруг бляшек при положительной фосфатазной пробе среда окрашивается в желтый цвет. Интенсивность окрашивания увеличивается через 18 - 24 часа - практически окрашивается вся среда.
4.5.4.4. Тест на наличие термостабильной дезоксирибонуклеазы (ДНКазы)
ДНКаза определяется по методу, основанному на метахроматических свойствах толуидина голубого. Этот метод диффузии в агар термостабильной ДНКазы St. aureus позволяет определить ее в концентрации примерно 0,005 мг/мл.
Среда: к 1000 мл 0,05 М трис-буфера (оксиметиламинометан) рН 9,0, добавляют 0,3 г ДНК, затем 10,0 г агара Дифко, 1 мл 0,01 М CaCl2. 10,0 г NaCl, 3,0 мл 0,1 М толуидина голубого. Среду разливают в пробирки по 12 - 15 мл, закрывают резиновыми пробками и хранят в холодильнике до 3 - 5 месяцев. Перед постановкой реакции среду растапливают и разливают в чашки Петри, подсушивают при 4 °С в течение 1 часа, вырезают лунки диаметром 3 мм, отсасывают пипеткой агар и вносят в лунки пастеровской пипеткой культуры, инкубируют при 37 °С.
Перед изучением культур пробирки с суточным ростом стафилококков на полужидком агаре прогревают в кипящей водяной бане 15 минут и вносят в лунки в агаровой пластинке, содержащей толуидин голубой. Зоны просветления с розовым окрашиванием образуются в результате гидролиза ДНК, находящейся в среде, термостабильной ДНКазой стафилококков. Проявление через 1 - 2 часа после внесения розовоокрашенных зон расценивается как положительная реакция на наличие термостабильной ДНКазы.
4.5.8. Идентификация стафилококков *(9)
*(9) - тесты на окисление маннита, термоустойчивую ДНКазу, кислую фосфатазу проводят в случае отрицательной реакции плазмокоагуляции.
Дифференцирующие признаки: (тесты)
Среди этимологических факторов пищевых токсикоинфекций существенную роль могут играть бактерии рода Proteus. Обнаружение небольших количеств протея в исследуемых продуктах не является поводом для подозрения его как возбудителя пищевого отравления. Однако, факт обнаружения протея является сигналом для проведения ряда санитарно-гигиенических и профилактических мероприятий на обследуемых объектах.
К роду Proteus относятся грамположительные бескапсульные в основном, подвижные бактерии, разжижающие желатину и расщепляющие мочевину, не образующие ацетилметилкарбинол и дающие положительную реакцию с метил-рот.
На основании различий по некоторым ферментативным свойствам возможна дифференциация рода Proteus на две биогруппы: Proteus vulgaris, который образует индол, ферментирует мальтозу и не декарбоксилирует орнитин, и Proteus mirabilis, который не образует индола, не ферментирует мальтозу и декарбоксилирует орнитин.
4.6.1. Методика выделения бактерий рода Proteus.
а) для получения чистой культуры первичный посев исследуемого материала из основного разведения (10 % взвесь) производят по 0,5 мл в конденсат свежескошенного агара по методу Шукевича.
На 2-й день просматривают посевы на скошенном МПА, если наблюдается вползающий нежный рост вуалеобразный рост, то с верхнего края выросшей культуры готовят препарат, окрашивают по Граму и микроскопируют. При наличии грамотрицательных полиформных палочек дают заключение о наличии бактерий рода Proteus в исследуемом продукте.
Кроме того, можно использовать посев на поверхность питательной среды Плоскирева или среды Вильсон-Блера, который производят в количествах 0,5 мл исходной взвеси, тщательно втирая шпателем, инкубируют при 37 °С 18 - 24 часа. На поверхности сред Плоскирева или Вильсон-Блера вырастает О-форм протея. Для получения из О-формы колоний Н-форм одну петлю суточной бульонной культуры протея наносят на поверхность свежеприготовленного 1,5 % МПА в центре чашки. Через 16 - 18 часов инкубирования при 37 °С наблюдается феномен «роения» - поверхность покрывается тонким слоем налета с голубоватым оттенком.
После инкубации в течение 18 - 24 часов при 37 °С чашки с посевами просматривают и отмечают колонии, подлежащие дальнейшему исследованию. На среде Плоскирева штаммы растут в виде прозрачных колоний, слегка подщелачивая среду, которая окрашивается вокруг них в желтоватый цвет. При более длительном хранении чашек с посевами колонии мутнеют, а центр их приобретает бурую окраску. На висмут-сульфитном агаре (среда Вильсон-Блера) через 48 часов штаммы вырастают в виде изолированных колоний грязно-коричневого цвета, окраска среды под колониями не изменяется.
Если рост 18 - 24 часовой культуры однородный, то для дальнейшего изучения используют не менее 3-х колоний. При росте разных колоний для их изучения надо брать больше колоний, различных по внешнему виду.
При наличии характерной микроскопической картины дают заключение о присутствии бактерий рода Proteus в исследуемом продукте *(10) .
*(10) - Идентификацию бактерий рода Proteus проводят в случае эпидситуации на объекте в соответствии с Инструкцией о порядке расследования, учета и проведения лабораторных исследований в учреждениях санэпидслужбы при пищевых отравления, Москва, 1975 г.
Случайные находки бактерий рода Proteus при определении бактерий группы кишечных палочек необходимо отражать в ответе.
В соответствии с рекомендациями ФАО/ВОЗ в большинстве пищевых продуктов нормируется отсутствие сальмонелл в определенной массе продукта. Сальмонеллы признаны индикаторными микроорганизмами при контроле пищевых продуктов на возможное присутствие патогенных микроорганизмов. В особо скоропортящейся продукции общественного питания сальмонеллы не допускаются в 25 г. Анализ проводят в соответствии с Инструкцией о порядке расследования, учета и проведения лабораторных исследований в учреждениях санитарно-эпидемиологической службы при пищевых отравлениях, Москва, 1975 г.
При текущем санитарном надзоре за предприятиями общественного питания и торговли, детскими и лечебными учреждениями исследование смывов проводят на присутствие бактерий группы кишечных палочек.
Исследование на наличие St. aureus, бактерий рода Рroteus, определение общей бактериальной обсемененности производится по показаниям. Например:
а) Исследование смывов на стафилококки проводят при обследовании кремово-кондитерских цехов, столовых и ресторанов, молочных кухонь и других пищеблоков, обращая особое внимание на контроль рук персонала;
б) общую микробную обсемененность можно определять для установления эффективности санитарной обработки посуды в посудомоечных машинах, а также при оценке новых моющих и дезинфицирующих средств.
В случае повторного обнаружения бактерий группы кишечных палочек в значительном проценте смывов на объекте рекомендуется провести исследование смывов с инвентаря, оборудования и рук персонала на наличие энтеробактерий *(11) .
*(11) - при исследовании смывов по эпидпоказаниям производят посев тампона и смывной жидкости на среды обогащения - селенитный бульон или магниевую среду (возможно использование сред Мюллера и Кауфмана). Дальнейшее выделение и идентификацию проводят согласно Инструкции о порядке расследования, учета и проведения лабораторных исследований в учреждениях санэпидслужбы при пищевых отравлениях, М. 1975.
5.2.1. Методика посева смывов на бактерии группы кишечных палочек
При плановых санитарно-гигиенических обследованиях для выявления БГКП производят посевы смывов на среды Кесслер с лактозой или КОДА, при этом в пробирку со средой опускают тампон и переносят оставшуюся смывную жидкость.
Посевы на средах Кесслер или КОДА инкубируют при 37 °С, через 18 - 24 часа со среды Кесслер производят высев на плотную дифференциальную среду Эндо, со среды КОДА высев производят только в случае изменения окраски среды или ее помутнения. Дальнейший ход исследования см. в п. 4.4.1.
5.2.2 Методика посева на общую бактериальную обсемененность
Для определения общей обсемененности поверхностей контролируемых предметов взятие смывов производят по методике, описанной выше (п. 4.3. ), перед посевом в пробирку с тампоном добавляют 5 мл 0,1 % пептонной воды или изотонического раствора хлорида натрия. Тампон тщательно отмывают, после чего 1,0 мл смывной жидкости помещают в чашку Петри и заливают расплавленным МПА. Чашки помещают в термостат при 30 °С. Предварительный подсчет выросших колоний производят через 48 часов, окончательный - через 72 часа. Количество колоний, выросших на чашке, умножают на 10 для определения общего количества бактерий, содержащихся на поверхности исследуемого предмета.
5.2.3. Методика посева на St. aureus
Для выявления St. aureus посев смывов производят на чашки с МСА или ЖСА, непосредственно втирая посевной материал тампоном, затем последний погружают в пробирку с 6,5 % солевым бульоном. Если необходимо определить и бактерии группы кишечных палочек, то остатки смывной жидкости переносят пипеткой в среды Кесслер или КОДА (п. 4.4.1.).
5.2.4. Оценка результатов
Обнаружение санитарно-показательных и условно-патогенных бактерий в смывах с поверхностей чистых, подготовленных к работе предметов, инвентаря и оборудования, а также рук персонала свидетельствует о нарушении санитарного режима и дает основание для проведения административных мер.
Для приготовления изотонического раствора с рН 6,9 - 7,0 используют дистиллированную воду, рН которой проверяют индикатором бромтимолблау, при его добавлении цвет воды должен быть бутылочно-зеленым. В иных случаях воду не используют. Изотонический раствор разливают в пробирки или флаконы в необходимых количествах, стерилизуют при 1 атм. 20 мин.
К 1 л дистиллированной воды добавляют 1 г пептона. После размешивания среду кипятят, фильтруют и разливают по пробиркам и флаконам в необходимых количествах, стерилизуют при 1 атм. 30 мин.
Довести рН до 7,0, разлить в пробирки по 15 мл, стерилизовать в течение 20 мин при 121 °С (1,1 атм).
К 1 л водопроводной воды прибавляют 10 г пептона и 50 мл желчи крупного рогатого скота, кипятят смесь при помешивании 20 - 30 мин в водяной бане и фильтруют через вату. В полученном фильтрате растворяют 2,5 г лактозы и доводят объем до 1 л, устанавливают реакцию среды (рН 7,4 - 7,6), после чего добавляют 2 мл 1 % водного раствора кристаллического фиолетового, разливают в пробирки по 5,0 мл, 10,0 мл и во флаконы по 50 мл. Готовая среда должна иметь темно-фиолетовый цвет. Среду стерилизуют при 1 атм. 10 мин, предварительно опустив в пробирки поплавки.
Среду готовят по прописи на этикетке. Разливают по 5 и 10 мл в пробирки без поплавков.
6.6. Бульон с лактозой, бычьей желчью и бриллиантовым зеленым - ЖЛБсухая бычья желчь
- 20 г (или 200 мл свежей фильтрованной желчи кр. рог. скота)
Растворяют пептон и лактозу в 500 мл дистиллированной воды, добавляют бычью желчь, растворенную в 200 мл воды, смешивают, доводят объем до 950 мл, рН до 7,4. Добавляют 13,3 мл 0,1 % водного раствора бриллиантового зеленого, доводят общий объем водой до 1 л. Разливают в пробирки с поплавками по 10 мл. Стерилизуют 115 мин при 121 °С.
6.7. ЕС-бульон (для подтверждающего посева на Е. coli по методу НВЧ) *(12)*(12) - Пропись ФАО/ВОЗ в модификации Института питания АМН СССР
Сухой панкреатический гидролизат казеина
- 20 г (или десятикратное количество жидкого ПГК с содержанием ок. 500 мг % аминного азота)
Растворяют ингредиенты, доводят рН до 6,9, разливают по 15 мл в пробирки с поплавками, стерилизуют в течение 15 мин при 121 °С.
На 1 л дистиллированной воды берется 10 г пептона, 5 г хлористого натрия, 2,5 г глюкозы. В дистиллированную воду в начале добавляют пептон, хлористый натрий и кипятят до растворения ингредиентов, затем добавляют 10 мл реактива Андреде. Устанавливают рН 7,2 - 7,4, добавляют углевод и фильтруют. Среду разливают в стерильные пробирки с поплавками по 2 - 3 мл. Стерилизуют при 0,5 атм 20 мин.
Приготовление индикатора Андреде:
Фуксин кислый в количестве 1 г растворяют в 200 мл дистиллированной воды, добавляют 32 мл нормального раствора едкого натра. Полученную смесь настаивают в течение 3-х суток при комнатной температуре или в течение суток при 37 °С, после чего фильтруют. Реактив хранят во флаконе с притертой пробкой.
Среды Эндо, Левина (эозинметиленовоголубой агар) выпускаются в сухом виде Дагестанским НИИ питательных сред, их следует готовить согласно прописям на этикетках банок. Изготовленные и разлитые в стерильные чашки Петри среды можно хранить при температуре 4 °С ± 1 °С до 10 суток.
6.10. Среда для определения индолообразованияСухой панкреатический гидролизат казеина
В случае отсутствия среды 6.10. используется для теста на индол.
Для приготовления бульона основной перевар Хоттингера разводят дистиллированной водой (или водопроводной) до содержания аминного азота 120 - 130 мг %, добавляют хлористый натрий в концентрации 0,5 %, K2 HPO4 - 0,1 %. Устанавливают рН 7,4 - 7,6 и кипятят 15 - 20 мин. Приготовленный бульон фильтруют через ватно-марлевый фильтр, разливают в пробирки по 5 - 8 мл. Стерилизуют при 1 атм. 20 мин.
Индикаторная бумажка на индол
Спирт этиловый 96°
фосфорная кислота (конц.)
Добавленные в спирт ингредиенты смешать до полного растворения. Полученной желтоватой жидкостью смочить край, приблизительной на 1/3, полоски фильтровальной бумаги. Цвет смоченного конца полоски бумаги должен быть желтым. При образовании индола изучаемой культурой цвет бумажки меняется от сиренево-розового до интенсивно-малинового.
6.12. Среда КларкаРастворить ингредиенты в 950 мл дистиллированной воды, добавить 10 мл 0,5 % спиртового раствора бромтимолового синего. Установить рН 6,8, проверяя значение рН на потенциометре. Довести объем дистиллированной водой до 1 л. Разлить в пробирки по 10 мл, стерилизовать в течение 15 мин при 121 °С.
Среда готовится аналогично среде Козера (6.15.), но после измерения рН в нее добавляют 20 г ± 0,1 г агар-агара на 1 л. Прогревают на водяной бане до растапливания агара, стерилизуют в течение 15 мин при 121 °С. Разливают в стерильные чашки Петри или пробирки.
К 100 мл горячей стерильной дистиллированной воды добавляют 4 г сухого препарата с индикатором ВР и лактозой, 0,1 г глюкозы и 1 г мочевины. Полученную среду разливают в стерильные пробирки по 5 - 6 мл и стерилизуют при 0,5 атм 20 мин. или текучим паром 2 дня подряд по 15 - 20 мин.
К 100 мл стерильного питательного агара добавляют 1 г лактозы, 0,02 г соли Мора, 0,3 г гипосульфита, 1 г сахарозы, 0,1 г глюкозы, 1 г мочевины, 0,4 % раствора фенолового красного 0,4 мл. Предварительно растворяют соль Мора с гипосульфитом в одной пробирке с небольшим количеством воды, а в другой - мочевину с углеводами. После растворения все смешивают с агаром и фильтруют через стерильную марлю. Стерилизуют текучим паром 3 дня подряд по 20 мин. Горячую среду скашивают в пробирках. Незасеянная среда имеет бледно-розовый цвет.
К 100 мл МПБ с рН 7,0 добавляют 6,5 г хлористого натрия. Разливают в пробирки по 5 мл и стерилизуют при 1 атм 20 мин.
К 100 мл стерильного бульона Хоттингера с рН 7,2 - 7,4 и содержанием 130 - 150 мг % аминного азота, добавляют глюкозу в количестве 1,0 г. После растворения среду разливают в пробирки по 5 мл и стерилизуют при 0,5 атм в течение 20 мин.
Стерильное молоко готовят из обезжиренного молока (кислотность 16 - 18 °Т), которое разливают в пробирки по 10 мл. Стерилизуют при 0,75 атм 15 мин. Обезжиренное молоко получают путем центрифугирования или кипячения с последующим отстаиванием в цилиндре в холодильнике в течение 2-х дней.
К 100 мл расплавленного и остуженного до 45 °С 2 % питательного агара с концентрацией 6,5 % хлористого натрия добавляют в количестве 10 мл стерильное обезжиренное молоко. Среду тщательно перемешивают и разливают по чашкам.
Желточно-солевой агар может быть приготовлен на основе сухого питательного агара, мясо-пептонного бульона или бульона Хоттингера.
При использовании МПБ к последнему добавляют 2 % агар-агара и 6,5 % хлористого натрия. При использовании бульона Хоттингера содержание аминного азота в нем должно составлять 150 мг %, для получения солевого агара добавляют 2 % агар-агара и 6,5 % хлористого натрия.
В случае использования сухого питательного агара к последнему добавляют 6,5 % хлористого натрия.
Солевой агар разливают во флаконы по 200 мл и стерилизуют при 1 атм 30 мин.
Приготовление рабочего раствора желтка:
На дно стерильной чашки помещают яйцо, которое тщательно протирают ватой, смоченной спиртом. Пинцетом пробивают с двух противоположных сторон яйца 2 отверстия. Через одно из этих отверстий из яйца полностью удаляют белок, а затем, несколько увеличив отверстие, выливают желток в стерильную банку с 5 - 6 бусинами. К желтку постепенно добавляют частями по 20 - 30 мл 180 - 200 мл стерильного изотонического раствора NaCl. Затем содержимое тщательно встряхивают.
На 100 мл расплавленного и остуженного до 45 °С солевого агара добавляют 20 мл рабочего раствора желтка. После полного размешивания агар в условиях бокса разливают в чашки по 15 - 17 мл. Чашки можно хранить в холодильнике до 1,5 - 2 недель.
К 100 мл 2 %-го расплавленного и остуженного до 45 °С питательного агара добавляют 10 мл стерильного снятого молока. После тщательного перемешивания агар выливают в чашки по 12 - 15 мл.
Цитратная плазма кролика для реакции плазмокоагуляции выпускается в сухом виде. Готовят непосредственно перед употреблением согласно прописи, прилагаемой в наставлении.
Среду готовят из сухого препарата с индикатором ВР и маннитом по прописи на этикетке. Среду разливают в пробирки по 12 - 15 мл.
Среду готовят по прописи на этикетке.
Среду готовят по прописи на этикетке. Изготовленную и разлитую в стерильные чашки Петри среду можно хранить в холодильнике при +4 °С до 10 суток.
Среду готовят из сухого препарата с индикатором ВР и мальтозой по прописи на этикетке. Среду разливают в пробирки по 2 - 3 мл.